 “E’ essenziale proteggere la biodiversità in quanto fonte di risorse, anche farmaceutiche, di grande valore per l’uomo“. “Lo studio dei metaboliti secondari di origine vegetale è estremamente importante per le prospettive legate al loro uso come farmaci, sia direttamente che attraverso lo sviluppo di lead compounds“. “Dalle fonti vegetali è possibile ottenere un gran numero di sostanze terapeuticamente valide“. “Gli ecosistemi marini e terrestri custodiscono vere e proprie farmacie, o meglio librerie di sostenze attive che l’uomo può sfruttare per curare le patologie più svariate. Queste molecole possono essere usate direttamente, indirettamente o fornire ispirazione strutturale per la sintesi di principi attivi“. Ed ancora “in un laboratorio farmaceutico medio oltre il 60% dei farmaci proviene, direttamente o indirettamente, dalle piante” mentre “un quarto delle prescrizioni rilasciate negli stati uniti d’America contiene principi attivi estratti da piante”.
“E’ essenziale proteggere la biodiversità in quanto fonte di risorse, anche farmaceutiche, di grande valore per l’uomo“. “Lo studio dei metaboliti secondari di origine vegetale è estremamente importante per le prospettive legate al loro uso come farmaci, sia direttamente che attraverso lo sviluppo di lead compounds“. “Dalle fonti vegetali è possibile ottenere un gran numero di sostanze terapeuticamente valide“. “Gli ecosistemi marini e terrestri custodiscono vere e proprie farmacie, o meglio librerie di sostenze attive che l’uomo può sfruttare per curare le patologie più svariate. Queste molecole possono essere usate direttamente, indirettamente o fornire ispirazione strutturale per la sintesi di principi attivi“. Ed ancora “in un laboratorio farmaceutico medio oltre il 60% dei farmaci proviene, direttamente o indirettamente, dalle piante” mentre “un quarto delle prescrizioni rilasciate negli stati uniti d’America contiene principi attivi estratti da piante”.
Si tratta di alcune espressioni classicamente usate nell’introdurre studi sulle sostanze bioattive di origine vegetale, pezze giustificative a lavori di ricerca o semplicemente frasi d’attacco per relazioni e conferenze sulla protezione o sull’utilizzo delle risorse naturali e sulla loro relazione con il mondo farmaceutico propriamente detto. Non parlano sempre della stessa cosa, anzi spesso prestano il fianco ad una certa confusione tra sostanze usate sic et simpliciter e sostanze naturali che forniscono l’ispirazione, lo scheletro di atomi da customizzare con mano umana per avere farmaci più efficaci. Queste affermazioni vengono talvolta corroborate da esempi reali più o meno attuali presi dal prontuario farmaceutico, come l’acido shikimico nella sintesi del Tamiflu (uno dei farmaci elettivi nel trattamento delle influenze virali tanto citate in questi mesi) o la metformina, l’aspirina, i glicosidi digitalici, il tassolo, i derivati della vinblastina, le statine e le ciclosporine (tutte figlie di mamma Natura anche se uscite dalle pipelines dell’industria farmaceutica e quindi spesso tacciate di apostasia), senza dimenticare l’esempio cardine di questa discussione sul legame farmaco-diversità biologica: gli antibiotici. Qual’è però l’entità reale del contributo messo a disposizione dalla chemodiversità naturale e come viene modulato? I numeri, vogliamo i numeri! Si tratta di affermazioni reali o di artifici retorici? Ovvero, escludendo le droghe vegetali ed i fitocomplessi impiegati in erboristeria e negli integratori alimentari, è possibile determinare quale peso hanno le sostanze di origine vegetale (meglio, di orgine vivente) nell’armamentario farmaceutico vero e proprio? Quello di pertinenza medica, composto da medicinali formati da molecole pure e definite, riconosciuti come tali dalle autorità e sviluppati dalle case farmaceutiche secondo l’iter pre-clinico e clinico, per intenderci. Non necessariamente prodotti in massa da piante o microrganismi, vanno bene anche quelli poi sintetizzati in laboratorio, purchè l’idea sia giunta al farmacologo per mimesi dell’esistente in natura.
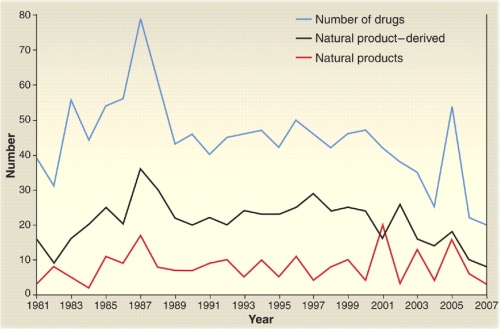
Per arrivare ai numeri, la prima spinta arriva da un articolo recente apparso su Science e da cui ho estrapolato questo grafico. Descrive l’andamento nel tempo delle registrazioni di nuovi farmaci negli Stati Uniti, siano essi di sintesi o di origine naturale più o meno diretta. Se ne evincono alcune cose interessanti a complemento di altre: la prima è che il numero dei nuovi farmaci registrati ogni anno è pari a poche decine, molto inferiore a quanto si potrebbe ipotizzare discutendone al bar con gli amici; la seconda è che questo numero è in costante calo da circa dieci anni; la terza è che almeno metà del totale vanta una liaison più o meno stretta con la natura e la quarta è che il rapporto tra “sintetico” e “naturale” è da considerarsi stabile nel tempo.
Le virgolette però sono come un cartello di pericolo generico sul ciglio della strada. Come altre volte, infatti, piazzare la staccionata è la cosa più complicata ed a seconda di dove piantiamo i paletti della discussione il paesaggio che si ottiene muta in maniera sensibile. Nel caso specifico il confine riguarda la distizione tra farmaco sintetico e farmaco di derivazione naturale: a seconda della loro definizione i rapporti del grafico di cui sopra possono prendere pieghe diverse. Una delle risposte più interessanti e solide a questo busillis viene da una serie di reviews portate avanti da l National Cancer Institute e pubblicate con regolarità nel 1997, nel 2003 e soprattutto nel 2007. Lo studio più recente ed interessante è questo (in pdf), redatto partendo dagli archivi dei farmaci registrati non solo negli USA e suddividendo i risultati in 5 categorie principali: farmaci ottenuti per sintesi de novo, ovvero senza alcun legame con molecole di origine/ispirazione naturale; farmaci ottenuti da molecole identiche a quelle estratte da esseri viventi (animali, piante o micororganismi); farmaci in cui la parte attiva è ispirata ad una struttura reperibile in natura ma oggetto di modifiche da parte dell’uomo (inclusi i vaccini) e farmaci in cui solo la parte non attiva è di origine naturale. In altre parole gli autori hanno definito “di origine naturale” qualunque farmaco contenente almeno una parte che mima, riproduce o prende ispirazione da una struttura presente anche in un essere vivente, fattore che considero idoneo per dare risposta alle domande di partenza.
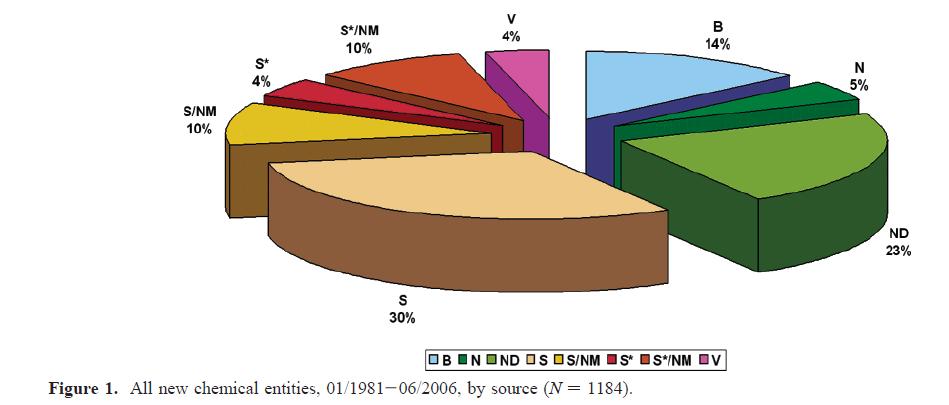
I numeri raccolti da Newman e Cragg sono riassunti nella torta che sta qui sotto e la probabilità di mordere una fetta in qualche modo ispirata alla chemodiversità naturale è del 70% circa. Non male, come suggeritore. Esistono tuttavia alcuni comparti farmaceutici nei quali il contributo del suggeritore naturale è molto limitato se non nullo: diuretici, antistaminici ed ipnotici sono praticamente tutti creati da una progettazione al 100% umana.
Leggendo l’articolo di Science emerge però anche un’altra realtà: la congiuntura sta imponendo un mutamento del modello della ricerca, strettamente dettato da esigenze economiche. Le aziende farmaceutiche hanno bisogno di rientri veloci ai loro investimenti e di grosse garanzie sulla brevettabilità delle loro ricerche. Due terreni su cui lo scandaglio della chemodiversità naturale cede il passo al controllo seriale ed automatizzato di strutture chimiche già note, attraverso l’uso della chimica combinatoriale ed alla rigorosa applicazione della regola di Lipinski (che non sempre vale per le molecole naturali). Cercare e riconoscere il veramente nuovo costa più che riprocessare il noto, è abbastanza lapalissiano. L’impasse però dovrebbe essere solo temporanea, legata alla fase economica contingente, perchè i numeri dicono che lavorare sulla chemodiversità costa di più ma garantisce probabilità di migliori dividendi a lungo termine. Un esempio: lavorare sui metaboliti a struttura polichetidica offre una probabilità dello 0,3% di giungere ad un principio attivo commerciabile contro lo 0,001% dello screening di librerie di composti noti. E dato che gli screening approfonditi del mondo che ci circonda hanno sinora coinvolto solo l’1% della flora microbica e circa il 15% della flora vegetale si capisce perchè anche dal punto di vista utilitaristico dell’industria farmaceutica evitare il depauperamento della diversità biologica è effettivamente buona cosa.
Manca, ma sarebbe interessante da fare, un diagramma che assegni il rispettivo fatturato ad ogni molecola inserita nei grafici che illustrano il post. Darebbe senso al valore (senso da declinare a piacere) della diversità ed alla perdita conseguente alla sua riduzione. Basti pensare che il best-seller mondiale degli ultimi anni è l’atorvastatina (Lipitor), una molecola prodotta per via sintetica ma ottenuta rielaborando radicalmente una struttura naturale. Se non fossero state precedentemente scoperte e studiate le statine di diretta produzione microbiologica, non avremmo avuto modo di sviluppare quelle più moderne ed efficaci (e redditizie) attualmente sul mercato.
Sempre ottimamente informativo, vorrei linkarlo nel mio vecchio post su uomini e piante, visto che anche il mio incipit era del tipo da te descritto 🙂
ciao
E chiedi anche il permesso? Vadi, vadi…
[…] tra farmaci prodotti e farmaci legati in maniera più o meno diretta al mondo vegetale vedi il post di […]
[…] il magazine mensile de Il Sole 24 Ore in edicola in questi giorni, in cui si toccano i temi della drug discovery a partire da dati etnomedici, dei problemi connessi alla qualità delle droghe vegetali per aziende […]
[…] alla natura facendo indagini chiamate bioprospezioni. Questa seconda via di drug-discovery, che come scritto non è affatto in disuso, può essere condotta in modalità random (provo tutte le piante che trovo, a caso, su tutte le […]
[…] kg per ettaro, sufficienti a curare circa 10.000 tra i 400 milioni di malati annui. Come sempre, non è la pianta a curare ma quel che ci sta dentro, come ben sapeva Youyou Tu quando ha avviato i suoi studi. Per questi motivi molti gruppi di ricerca […]